მოლეკულური ბიოლოგიის ტექნოლოგიის უწყვეტი განვითარებით, გენის მუტაციებსა და დეფექტებსა და დაავადებებს შორის ურთიერთობა უფრო და უფრო ღრმა გაგებას იძენს.ნუკლეინის მჟავებმა დიდი ყურადღება მიიპყრო დაავადებების დიაგნოსტიკასა და მკურნალობაში გამოყენების დიდი პოტენციალის გამო.ნუკლეინის მჟავას პრეპარატები ეხება ხელოვნურად სინთეზირებულ დნმ-ის ან რნმ-ის ფრაგმენტებს დაავადების სამკურნალო ფუნქციებით.ასეთ პრეპარატებს შეუძლიათ უშუალოდ იმოქმედონ დაავადების გამომწვევ სამიზნე გენებზე ან დაავადების გამომწვევ სამიზნე mRNA-ებზე და შეასრულონ როლი გენის დონეზე დაავადებების მკურნალობაში.ტრადიციულ მცირე მოლეკულურ პრეპარატებთან და ანტისხეულებთან შედარებით, ნუკლეინის მჟავას პრეპარატებს შეუძლიათ დაარეგულირონ დაავადების გამომწვევი გენების გამოხატულება ძირიდან და აქვთ „სიმპტომების მკურნალობა და ძირეული მიზეზის განკურნება“.ნუკლეინის მჟავას პრეპარატებს ასევე აქვთ აშკარა უპირატესობები, როგორიცაა მაღალი ეფექტურობა, დაბალი ტოქსიკურობა და მაღალი სპეციფიკა.მას შემდეგ, რაც 1998 წელს გამოუშვეს პირველი ნუკლეინის მჟავა პრეპარატი fomivirsen sodium, მრავალი ნუკლეინის მჟავა პრეპარატი დამტკიცებულია კლინიკური მკურნალობისთვის.
ნუკლეინის მჟავას პრეპარატები, რომლებიც ამჟამად ბაზარზეა გლობალურად, ძირითადად მოიცავს ანტისენსუს ნუკლეინის მჟავას (ASO), მცირე ინტერფერენტულ რნმ-ს (siRNA) და ნუკლეინის მჟავას აპტამერებს.გარდა ნუკლეინის მჟავების აპტამერებისა (რომლებიც შეიძლება აღემატებოდეს 30 ნუკლეოტიდს), ნუკლეინის მჟავას პრეპარატები, როგორც წესი, არის ოლიგონუკლეოტიდები, რომლებიც შედგება 12-დან 30 ნუკლეოტიდისგან, რომლებიც ასევე ცნობილია როგორც ოლიგონუკლეოტიდური პრეპარატები.გარდა ამისა, miRNA-ებმა, რიბოციმებმა და დეზოქსირიბოზიმებმა ასევე აჩვენეს განვითარების დიდი მნიშვნელობა სხვადასხვა დაავადების სამკურნალოდ.ნუკლეინის მჟავას პრეპარატები დღეს ბიომედიცინის კვლევისა და განვითარების ერთ-ერთ ყველაზე პერსპექტიულ სფეროდ იქცა.
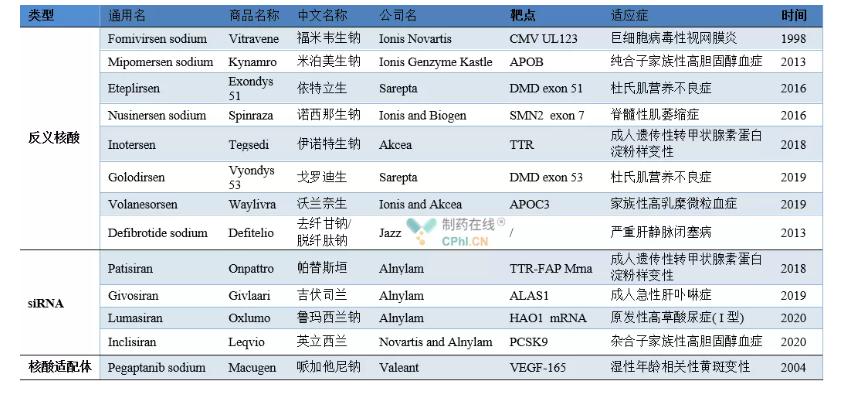
ნუკლეინის მჟავას დამტკიცებული პრეპარატების მაგალითები
ანტისენსიური ნუკლეინის მჟავა
Antisense ტექნოლოგია არის წამლის განვითარების ახალი ტექნოლოგია, რომელიც დაფუძნებულია Watson-Crick-ის ბაზის კომპლემენტაციის პრინციპზე, ორგანიზმის მიერ ხელოვნურად სინთეზირებული ან სინთეზირებული სპეციფიკური დამატებითი დნმ-ის ან რნმ-ის ფრაგმენტების გამოყენებით სამიზნე გენების ექსპრესიის სპეციალურად დასარეგულირებლად.ანტიმგრძნობიარე ნუკლეინის მჟავას აქვს სამიზნე რნმ-ის შემავსებელი ბაზის თანმიმდევრობა და შეუძლია მას კონკრეტულად დაუკავშირდეს.ანტიმგრძნობიარე ნუკლეინის მჟავები ზოგადად შეიცავს ანტისენსურ დნმ-ს, ანტისენსურ რნმ-ს და რიბოციმებს.მათ შორის, ანტისენსიური დნმ-ის მაღალი სტაბილურობისა და დაბალი ღირებულების მახასიათებლების გამო, ანტისენსიური დნმ დომინანტურ პოზიციას იკავებს ანტისენსიური ნუკლეინის მჟავას პრეპარატების მიმდინარე კვლევასა და გამოყენებაში.
Fomivirsen sodium (სავაჭრო სახელი Vitravene) შეიქმნა Ionis Novartis-ის მიერ.1998 წლის აგვისტოში FDA-მ დაამტკიცა ის ციტომეგალოვირუსული რეტინიტის სამკურნალოდ იმუნოდეფიციტის მქონე პაციენტებში (ძირითადად შიდსით დაავადებულ პაციენტებში), რაც გახდა პირველი ნუკლეინის მჟავის პრეპარატი, რომელიც ბაზარზე გამოვიდა.ფომივირსენი აინჰიბირებს CMV ცილის ნაწილობრივ გამოხატვას სპეციფიკურ mRNA-სთან (IE2) მიერთებით, რითაც არეგულირებს ვირუსული გენების ექსპრესიას თერაპიული ეფექტის მისაღწევად.თუმცა, მაღალი ეფექტურობის ანტირეტროვირუსული თერაპიის გამოჩენის გამო, რამაც მნიშვნელოვნად შეამცირა პაციენტების რაოდენობა, 2002 და 2006 წლებში Novartis-მა გააუქმა Fomivirsen-ის წამლების ბაზარზე ავტორიზაცია ევროპასა და შეერთებულ შტატებში, შესაბამისად, პროდუქტი შეჩერდა ბაზრიდან.
Mipomersen sodium (სავაჭრო სახელი Kynamro) არის ASO პრეპარატი, რომელიც შემუშავებულია ფრანგული კომპანია Genzyme-ის მიერ.2013 წლის იანვარში FDA-მ დაამტკიცა ის ჰომოზიგოტური ოჯახური ჰიპერქოლესტერინემიის სამკურნალოდ.მიპომერსენი აფერხებს ApoB-100 ცილის (აპოლიპოპროტეინის) ექსპრესიას ApoB-100mRNA-სთან შეკავშირებით, რითაც მნიშვნელოვნად ამცირებს ადამიანის დაბალი სიმკვრივის ლიპოპროტეინის ქოლესტერინს, დაბალი სიმკვრივის ლიპოპროტეინს და სხვა ინდიკატორებს, მაგრამ გვერდითი ეფექტების გამო, როგორიცაა ღვიძლის ტოქსიკურობა. .
2016 წლის სექტემბერში, Eteplirsen (სავაჭრო სახელწოდება Exon 51) შემუშავებული Sarepta-ს მიერ დუშენის კუნთოვანი დისტროფიის (DMD) სამკურნალოდ დამტკიცებული იქნა FDA-ს მიერ.DMD პაციენტებს ჩვეულებრივ არ შეუძლიათ გამოხატონ ფუნქციური ანტიატროფიული პროტეინი ორგანიზმში DMD გენის მუტაციების გამო.ეტეპლირსენი სპეციალურად უკავშირდება ცილის წინასწარ მესინჯერის რნმ-ის (Pre-mRNA) ეგზონ 51-ს, შლის ეგზონ 51-ს და აღადგენს ზოგიერთ ქვედა დინებაში გენს.
Nusinersen არის ASO პრეპარატი, რომელიც შემუშავებულია Spinraza-ს მიერ ზურგის კუნთოვანი ატროფიის სამკურნალოდ და დამტკიცებულია FDA-ს მიერ 2016 წლის 23 დეკემბერს. 2018 წელს Tegsedi-ის მიერ შემუშავებული ინოტესენი ზრდასრულთა მემკვიდრეობითი ტრანსთირეტინ ამილოიდოზის სამკურნალოდ დამტკიცებული იყო FDA-ს მიერ.2019 წელს, გოლოდირსენი, რომელიც შეიქმნა Sarepta-ს მიერ დუშენის კუნთოვანი დისტროფიის სამკურნალოდ, დამტკიცებული იქნა FDA-ს მიერ.მას აქვს იგივე მოქმედების მექანიზმი, როგორც Eteplirsen, და მისი მოქმედების ადგილი ხდება ეგზონი 53. იმავე წელს Volanesorsen, ერთობლივად შემუშავებული Ionisand Akcea-ს მიერ ოჯახური ჰიპერქილომიკრონემიის სამკურნალოდ, დამტკიცებული იქნა ევროპის მედიკამენტების სააგენტოს (EMA) მიერ.ვოლანსორსენი არეგულირებს ტრიგლიცერიდების მეტაბოლიზმს აპოლიპოპროტეინის C-Ⅲ გამომუშავების ინჰიბირებით, მაგრამ მას ასევე აქვს გვერდითი ეფექტი - ამცირებს თრომბოციტების დონეს.
დეფიბროტიდი არის ოლიგონუკლეოტიდური ნარევი პლაზმინის თვისებებით, რომელიც შემუშავებულია ჯაზის მიერ.იგი შეიცავს 90% დნმ-ს ერთჯაჭვიან დნმ-ს და 10% ორჯაჭვიან დნმ-ს.ის დაამტკიცა EMA-მ 2013 წელს და შემდგომში დაამტკიცა FDA-ს მიერ ღვიძლის მძიმე ვენების სამკურნალოდ.ოკლუზიური დაავადება.დეფიბროტიდს შეუძლია გაზარდოს პლაზმინის აქტივობა, გაზარდოს პლაზმინოგენის აქტივატორი, ხელი შეუწყოს თრომბომოდულინის რეგულაციას და შეამციროს ფონ ვილბრანდის ფაქტორის და პლაზმინოგენის აქტივატორის ინჰიბიტორების ექსპრესია თერაპიული ეფექტის მისაღწევად.
siRNA
siRNA არის რნმ-ის მცირე ფრაგმენტი სპეციფიკური სიგრძით და თანმიმდევრობით, რომელიც წარმოიქმნება სამიზნე რნმ-ის ჭრის შედეგად.ამ siRNA-ებს შეუძლიათ კონკრეტულად გამოიწვიონ სამიზნე mRNA-ს დეგრადაცია და მიაღწიონ გენის გაჩუმებას.ქიმიურ მცირე მოლეკულურ პრეპარატებთან შედარებით, siRNA პრეპარატების გენის გამაჩუმებელ ეფექტს აქვს მაღალი სპეციფიკა და ეფექტურობა.
2018 წლის 11 აგვისტოს, პირველი siRNA წამალი patisiran (სავაჭრო სახელი Onpattro) დაამტკიცა FDA-მ და ოფიციალურად გამოუშვა.ეს არის ერთ-ერთი მთავარი ეტაპი რნმ-ის ჩარევის ტექნოლოგიის განვითარების ისტორიაში.Patisiran ერთობლივად შეიმუშავეს Alnylam-მა და Genzyme-მა, Sanofi-ს შვილობილი კომპანია.ეს არის siRNA პრეპარატი მემკვიდრეობითი თიროქსინით განპირობებული ამილოიდოზის სამკურნალოდ.2019 წელს გივოსირანი (სავაჭრო სახელი გივლაარი) დაამტკიცა FDA-მ, როგორც მეორე siRNA წამალი მოზრდილებში ღვიძლის მწვავე პორფირიის სამკურნალოდ.2020 წელს ალნილამმა შეიმუშავა პირველადი ტიპის I პრეპარატი ბავშვებისა და მოზრდილების სამკურნალოდ.ლუმასირანი მაღალი ოქსალურიით დამტკიცებული იყო FDA-ს მიერ.2020 წლის დეკემბერში, ინკლისირანი, რომელიც ერთობლივად იქნა შემუშავებული Novartis-ისა და Alnylam-ის მიერ მოზრდილთა ჰიპერქოლესტერინემიის ან შერეული დისლიპიდემიის სამკურნალოდ, დამტკიცებული იქნა EMA-ს მიერ.
აპტამერი
ნუკლეინის მჟავების აპტამერები არის ოლიგონუკლეოტიდები, რომლებსაც შეუძლიათ შეაერთონ სხვადასხვა სამიზნე მოლეკულები, როგორიცაა მცირე ორგანული მოლეკულები, დნმ, რნმ, პოლიპეპტიდები ან ცილები მაღალი აფინურობითა და სპეციფიკით.ანტისხეულებთან შედარებით, ნუკლეინის მჟავას აპტამერებს აქვთ მარტივი სინთეზის მახასიათებლები, დაბალი ღირებულება და მიზნების ფართო სპექტრი და აქვთ წამლის გამოყენების უფრო ფართო პოტენციალი დაავადების დიაგნოსტიკაში, მკურნალობასა და პრევენციაში.
პეგაპტანიბი არის პირველი ნუკლეინის მჟავას აპტამერი პრეპარატი, რომელიც შეიქმნა Valeant-ის მიერ სველი ასაკთან დაკავშირებული მაკულარული დეგენერაციის სამკურნალოდ და დამტკიცებული იქნა FDA-ს მიერ 2004 წელს. შემდგომში, ის დამტკიცებული იქნა EMA-სა და PMDA-ს მიერ 2006 წლის იანვარში და 2008 წლის ივლისში და გამოვიდა ბაზარზე.პეგაპტანიბი თრგუნავს ანგიოგენეზს სივრცითი სტრუქტურისა და სისხლძარღვთა ენდოთელური ზრდის ფაქტორის კომბინაციით თერაპიული ეფექტის მისაღწევად.მას შემდეგ იგი შეექმნა კონკურენციას მსგავსი პრეპარატების Lucentis-ისგან და მისი წილი ბაზარზე საკმაოდ დაეცა.
ნუკლეინის მჟავას წამლები გახდა ცხელი წერტილი კლინიკური წამლებისა და ახალი წამლების ბაზარზე მათი შესანიშნავი სამკურნალო ეფექტისა და განვითარების მოკლე ციკლის გამო.როგორც განვითარებადი ნარკოტიკი, ის გამოწვევების წინაშე დგას შესაძლებლობების წინაშე.მისი ეგზოგენური მახასიათებლების გამო, ნუკლეინის მჟავების სპეციფიკა, სტაბილურობა და ეფექტური მიწოდება გახდა მთავარი კრიტერიუმი იმის დასადგენად, შეიძლება თუ არა ოლიგონუკლეოტიდები გახდეს ძალიან ეფექტური ნუკლეინის მჟავა პრეპარატები.მიზანმიმართული ეფექტები ყოველთვის იყო ნუკლეინის მჟავების წამლების მთავარი პუნქტი, რომლის იგნორირება შეუძლებელია.თუმცა, ნუკლეინის მჟავას პრეპარატებს შეუძლიათ გავლენა მოახდინონ დაავადების გამომწვევი გენების გამოხატულებაზე ფესვიდან და შეუძლიათ მიაღწიონ თანმიმდევრობის სპეციფიკას ერთბაზის დონეზე, რომელსაც აქვს „ძირეული მიზეზის მკურნალობა და სიმპტომების მკურნალობა“.უფრო და უფრო მეტი დაავადების ცვალებადობის გათვალისწინებით, მხოლოდ გენეტიკურ მკურნალობას შეუძლია მუდმივი შედეგების მიღწევა.დაკავშირებული ტექნოლოგიების უწყვეტი გაუმჯობესებით, სრულყოფითა და პროგრესით, ნუკლეინის მჟავას პრეპარატები, რომლებიც წარმოდგენილია ანტისენსიური ნუკლეინის მჟავებით, siRNA და ნუკლეინის მჟავების აპტამერებით, აუცილებლად წამოიწყებენ ახალ ტალღას დაავადების მკურნალობასა და ფარმაცევტულ ინდუსტრიაში.
Rცნობები:
[1] Liu Shaojin, Feng Xuejiao, Wang Junshu, Xiao Zhengqiang, Cheng Pingsheng.ნუკლეინის მჟავას პრეპარატების ბაზრის ანალიზი ჩემს ქვეყანაში და კონტრზომები [J].ბიოლოგიური ინჟინერიის ჩინური ჟურნალი, 2021, 41 (07): 99-109.
[2] ჩენ ვენფეი, ვუ ფუხუა, ჟანგ ჟირონგი, სუნ ქსუნი.კვლევის პროგრესი ნუკლეინის მჟავების ბაზარზე გასაყიდი წამლების ფარმაკოლოგიაში[J].ჩინური ჟურნალი ფარმაცევტიკა, 2020, 51 (12): 1487-1496.
[3] ვანგ ჯუნი, ვანგ ლანი, ლუ ჯიაჟენი, ჰუანგ ჟენი.ნუკლეინის მჟავას პრეპარატების [J] ეფექტურობისა და კვლევის პროგრესის ანალიზი.ახალი წამლების ჩინური ჟურნალი, 2019, 28(18): 2217-2224.
ავტორის შესახებ: შა ლუო, ჩინური მედიცინის კვლევისა და განვითარების თანამშრომელი, ამჟამად მუშაობს წამლების კვლევისა და განვითარების დიდ ადგილობრივ კომპანიაში და ერთგულია ახალი ჩინური მედიკამენტების კვლევისა და განვითარებისთვის.
Მსგავსი პროდუქტები:
გამოქვეყნების დრო: ნოე-19-2021